热门靶点 TIGIT:百济再报三项临床,信达、君实、复宏汉霖均布局
10月27日,CDE官网显示,百济神州1类新药BGB-A1217注射液临床申请获受理。截至当前,百济已就BGB-A1217向NMPA提交共计4项临床申请,其与PD-1抗体百泽安(替雷利珠单抗)联合针对癌症的1/1b期临床已在澳大利亚启动。
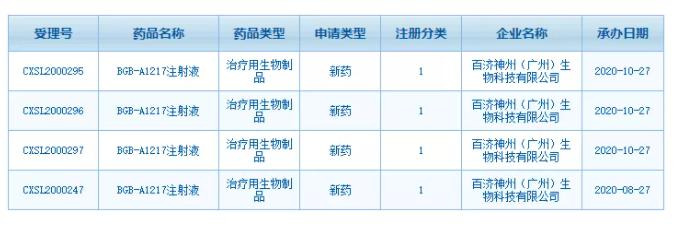
文章图片均来自原文:Insight数据库
免疫组合疗法:疗效优势显著
BGB-A1217是百济自主研发的一款TIGIT单抗。据百济投资者会议中的披露信息,其具有完整Fc功能,临床前研究中较罗氏同靶点单抗Tiragolumab活性强约4倍,且已确定了II期临床推荐剂量,在国内同靶点布局企业中居于领先地位。
目前,百济神州已启动一项BGB-A1217联合替雷利珠单抗用于治疗晚期实体瘤患者的1/1b期多中心临床试验(NCT04047862)。研究显示,该联合疗法一般耐受良好,无剂量限制性毒性(DLT)。
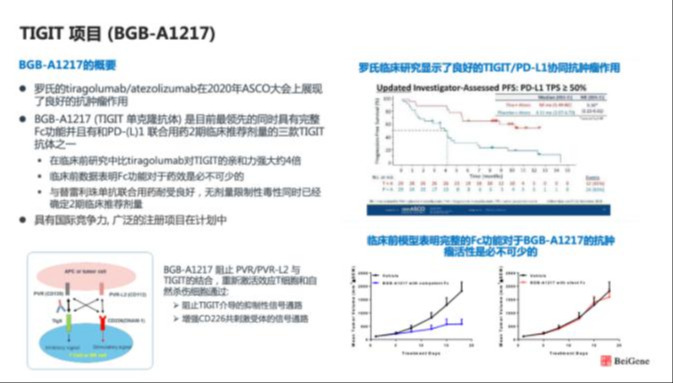
百济神州公开ppt资料
TIGIT是脊髓灰质炎病毒受体(PVR)/Nectin家族的成员,可通过与其同源配体PVR的结合,直接抑制淋巴细胞的激活。TIGIT和PVR广泛表达在不同类型的实体瘤中,是继PD-1/PD-L1之后的新型免疫检查点,在肿瘤免疫抑制中的作用和PD-1/L1类似。研究表明,TIGIT抑制剂和PD-1/L1抑制剂可发挥协同抗肿瘤作用。
当前,全球范围内,TIGIT靶点进展最快的为罗氏的Tiragolumab,已进展至III期临床。
2020年的ASCO大会中,罗氏报道了Tiragolumab与阿替利珠单抗(Tecentriq,PD-L1单抗)联合用药在非小细胞肺癌(NSCLC)患者中的CITYSCAPE临床研究结果。
CITYSCAPE研究是一项全球多中心、随机、双盲的2期临床,旨在评估Tiragolumab与Tecentriq联合一线治疗PD-L1阳性转移性或局部晚期不可切除NSCLC患者的疗效。
结果显示,与仅接受Tecentriq治疗的患者组对比,TIGIT+PD-L1组合疗法显示出了显著的改善:在意向性治疗(ITT)患者群体中,ORR达到31.3%,而Tecentriq单药患者组仅16.2%;PFS为5.4个月,而Tecentriq单药组仅3.6个月;同时,患者疾病恶化或死亡风险降低43%。
此外,在PD-L1高表达的患者群中,与单独使用Tecentriq的ORR为17.2%相比,组合疗法使患者的ORR达到55.2%,将患者的疾病恶化或死亡风险降低了67%。
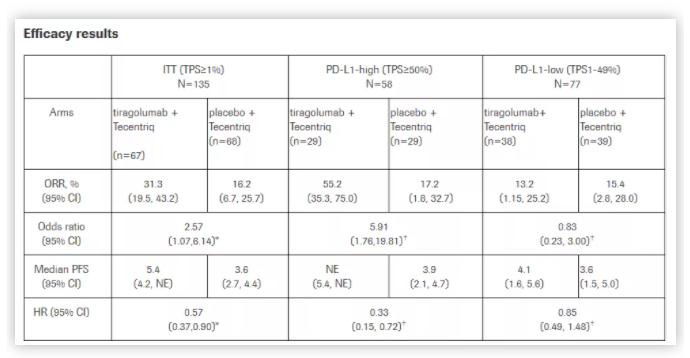
来自:罗氏制药
在安全性方面,Tecentriq单药与两种免疫疗法联合用药的不良事件发生率相近。联合疗法中,与治疗相关的AE(TRAE)发生率为80.6%,3级以上的TRAE发生率为14.9%;单独使用Tecentriq的亚组中,TRAE发生率为72%,3级以上为19.1%。
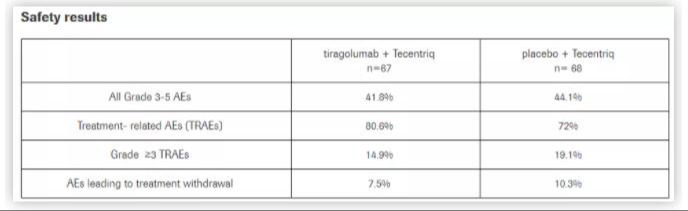
来自:罗氏制药
国内外多企业竞相布局
相关研究的积极结果,使TIGIT靶点倍受国内外众多药企的青睐。Insight数据库显示,在国外,罗氏、BMS、默沙东等知名药企已纷纷入局;而国内企业中,除百济之外,信达、君实、复宏汉霖等企业也均在此领域开始布局。
信达,IBI939
IBI939是由信达研发的国内首个TIGIT抗体,可与TIGIT结合并阻断其与CD155的相互作用,增强免疫活化。
2020年1月6日,Insight数据库显示,信达的1类新药IBI939获批临床,拟用于治疗晚期肿瘤(血液肿瘤和实体瘤);4月20日,信达启动IBI939单药及联合信迪利单抗治疗晚期恶性肿瘤的I期临床。
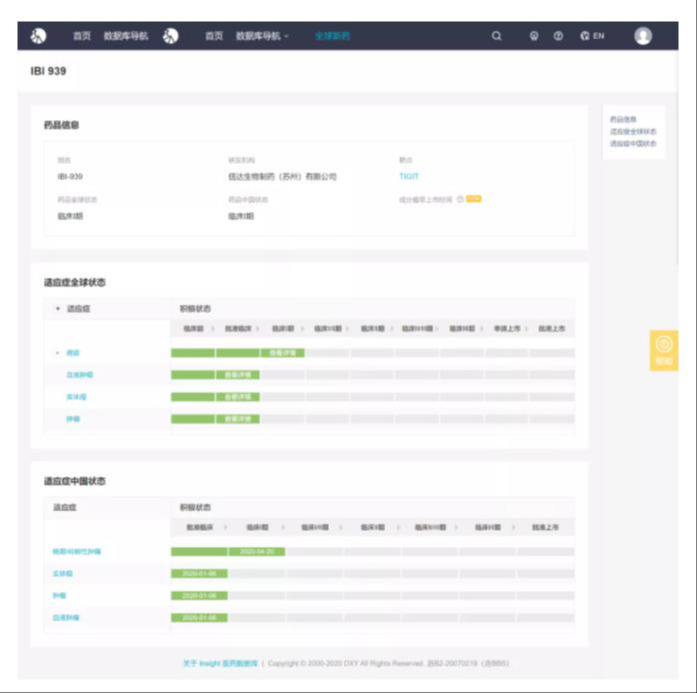
来自:Insight数据库君实,JS006
Insight数据库显示,目前君实的TIGIT单抗JS006尚处于临床前研究阶段,拟用于血液瘤和实体瘤。
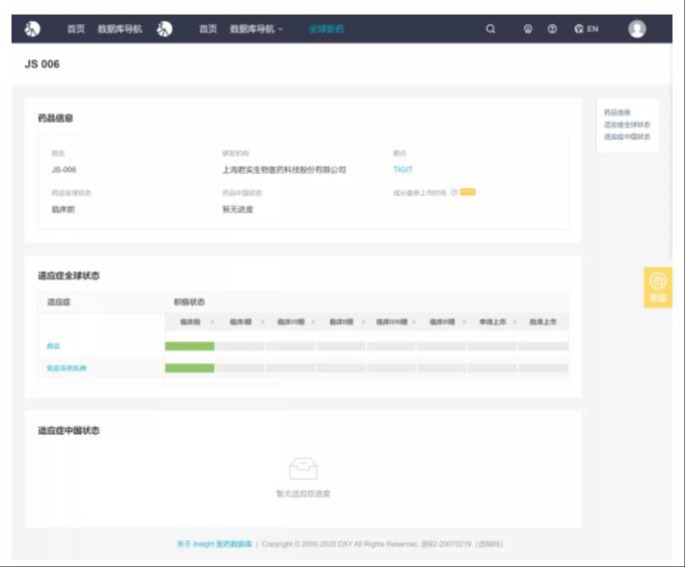
来自:Insight数据库
复宏汉霖:TIGIT单抗HLX53+双抗HLX301
复宏汉霖针对TIGIT靶点同时开发了单抗HLX53和双抗HLX301,均为纳米抗体。目前,该两款抗体尚处于临床前研究阶段。
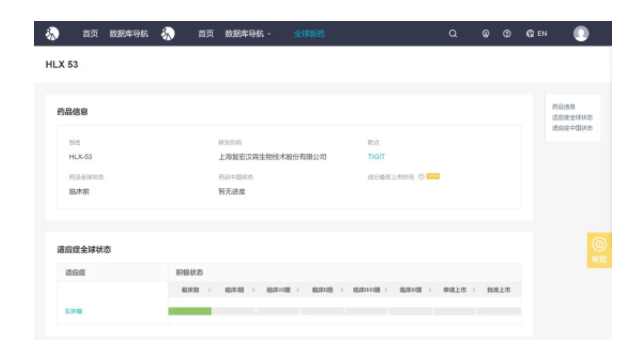
本文转自https://med.sina.com网站,若有侵权,请联系我们删除