迈威生物 (688062.SH),一家全产业链布局的创新型生物制药公司,2024 年 3 月 12 至 15 日在第 14 届世界抗体药物偶联大会 (World ADC London) 以壁报的形式发表 “Mtoxin™ Payload Applied in IDDC™ ADC Platform Significant Increases Therapeutic Index and Overcome MultiDrug Resistance in Various Tumor”,展示了新一代 ADC 技术平台 IDDC™ 赋能下多款 ADC 药物的开发情况。
壁报内容概述
新型偶联技术、释放技术以及新型毒素的广泛应用促使 ADC 领域蓬勃发展,然而进一步提升药物传递效率以及克服肿瘤耐药是下一代 ADC 药物亟待解决的问题,迈威生物自主开发了 IDDC™ 技术以及新型载荷 Mtoxin™。研究结果显示:
1. DARfinity™产生DAR 4为主成分的定点偶联药物(DAR 4≧95%)
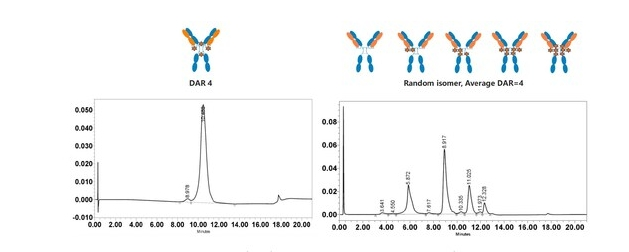
2. IDconnect™提升ADC药物血浆稳定性,提高载荷传递效率(相对对照组提升40%)
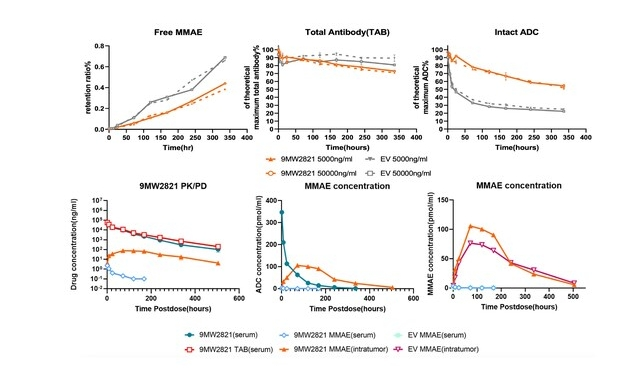
3. LysOnly™技术提升ADC药物的肿瘤特异性释放能力,降低脱靶效应
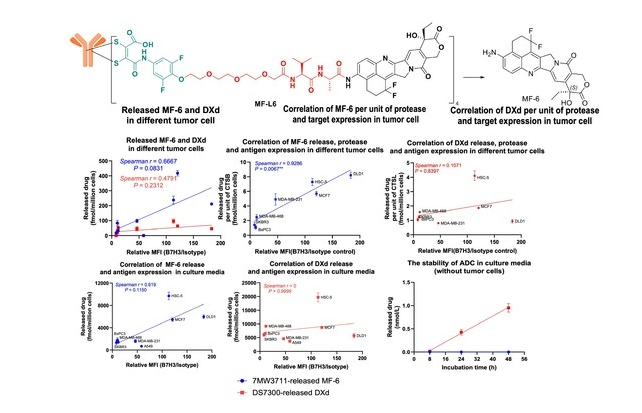
4. Mtoxin™具有良好的肿瘤穿透性、旁观者杀伤效果以及抗多药耐药特性
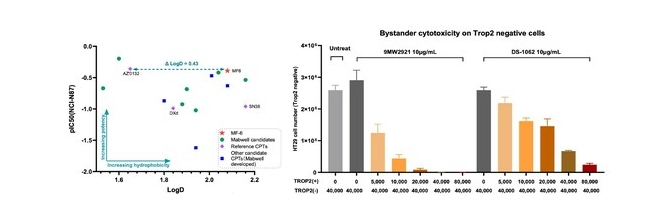
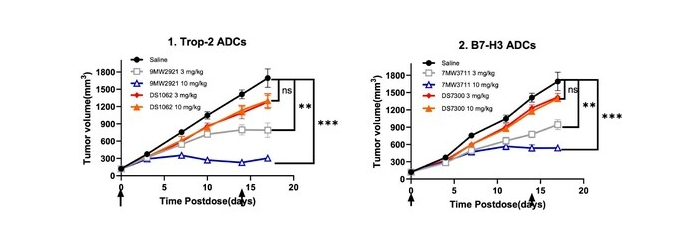
5. IDDC™与Mtoxin™构建的ADC药物具有良好的药效及安全性特性,特别在DXd耐药的多药耐药模型中,具有良好的药效
总结
IDDC™ 是一项经过临床验证的定点偶联技术,构建的 ADC 具有良好的均一性、有效性以及安全性优势。此外,新型载荷 Mtoxin™ (MF6) 具有良好的药效,旁观者杀伤效果,以及抗多药耐药等优势。
基于 IDDC™ 平台开发的 ADC 创新药
目前 IDDC™ 平台已在多个在研品种中得到验证。
靶向 Nectin-4 ADC 创新药 9MW2821
该品种针对尿路上皮癌适应症是国内企业首家进入 III 期临床研究且全球进度第二;亦是全球同靶点药物中首款在宫颈癌和食管癌适应症披露临床有效性和安全性数据的治疗药物。已获 FDA 快速通道认定用于治疗晚期、复发或转移性食管鳞癌。
靶向 B7-H3 ADC 创新药 7MW3711
该品种已开展针对晚期实体瘤适应症的临床试验,并获 FDA 批准针对晚期恶性实体瘤患者开展临床试验。
靶向 Trop-2 ADC 创新药 9MW2921
该品种已开展针对晚期实体瘤适应症的临床试验。
关于迈威生物
迈威生物 (688062.SH) 是一家全产业链布局的创新型生物制药公司,始终秉承“让创新从梦想变成现实”的愿景,践行“探索生命,惠及健康”的使命,通过源头创新,为患者提供疗效更好、可及性更强的生物创新药,满足全球未被满足的临床需求。2017 年成立以来,迈威生物构建了以抗体药物靶点发现与分子发现为起点,覆盖成药性研究、临床前研究、临床研究和生产转化等药品研发全周期的创新体系,实现集研发、生产、营销于一体的全产业链布局。我们专注于肿瘤和年龄相关疾病,涉及肿瘤、自身免疫、代谢、眼科、感染等治疗领域,凭借国际领先的特色技术平台和研发创新能力,建立了丰富且具有竞争力的管线。现有 14 个品种处于不同阶段,包括 10 个创新品种和 4 个生物类似药,其中 2 个品种上市,2 个品种药品上市许可申请已获受理,3 个品种处于关键注册临床试验阶段。并独立承担 1 项国家“重大新药创制”重大科技专项、2 项国家重点研发计划和多个省市级科技创新项目。迈威生物以创新为本,注重产业转化,符合中国 NMPA、美国 FDA、欧盟 EMA GMP标准的抗体和重组蛋白药物产业化基地已在江苏泰州投入使用,并已通过欧盟 QP 审计,位于上海金山和江苏泰州的大规模商业化生产基地正在建设中。欲了解更多信息,请访问:www.mabwell.com。
前瞻性声明
本新闻稿所发布的信息中可能会包含某些前瞻性表述。这些表述本质上具有相当风险和不确定性。在使用“预期”、“相信”、“预测”、“期望”、“打算”及其他类似词语进行表述时,凡与本公司有关的,目的均是要指明其属前瞻性表述。本公司并无义务不断地更新这些预测性陈述。
这些前瞻性表述乃基于本公司管理层在做出表述时对未来事务的现有看法、假设、期望、估计、预测和理解。这些表述并非对未来发展的保证,会受到风险、不确性及其他因素的影响,有些乃超出本公司的控制范围,难以预计。因此,受我们的业务、竞争环境、政治、经济、法律和社会情况的未来变化及发展的影响,实际结果可能会与前瞻性表述所含资料有较大差别。
本公司、本公司董事及雇员代理概不承担 (a) 更正或更新本网站所载前瞻性表述的任何义务;及 (b) 若因任何前瞻性表述不能实现或变成不正确而引致的任何责任。







